الماء سر الحياة
أَوَلَمْ يَرَ الَّذِينَ كَفَرُوا أَنَّ السَّمَاوَاتِ وَالْأَرْضَ كَانَتَا رَتْقًا فَفَتَقْنَاهُمَا وَجَعَلْنَا مِنَ الْمَاءِ كُلَّ شَيْءٍ حَيٍّ أَفَلَا يُؤْمِنُونَ (30)
سورة الأنبياء
كلنا نعلم أن الماء يعني الحياة وبدون ماء لا شيء يمكن أن يبقى على قيد الحياة.
لو فقدنا 4% من حجم الماء في جسمنا سنعاني من أعراض الجفاف، ولو فقدنا 15% فإن حياتنا تصبح في خطر شديد.
لا نستطيع العيش أكثر من ثلاث أيام بدون ماء بينما يمكن أن نعيش لمدة شهر بدون طعام.
من الممكن أن تتواجد الحياة بدون أكسجين، فهناك الكائنات وحيدة الخلية مثل أنواع البكتيريا الزرقاء (Cyanobacteria or blue-green algae) وأنواع من البكتيريا القديمة (Archaea) التي يمكن أن تعيش من دون الأكسجين، وعوضاً عن الأكسجين فإنها “تتنفس” (بالطبع هذا لا يشبه تنفسنا، لأن هذه الكائنات وحيدة الخلية ليس لها رئة)عناصر أخري مثل الحديد، هذه العناصر هي مستقبلات الإلكترونات.
وحديثاً أكتشف العلماء أنواع من الكائنات متعددة الخلايا تعيش بدون أكسجين بعض منها الطفيليات التي يبدو أنها تخلصت من أجهزة أنتاج الطاقة (Mitochondria) وبطريقة ما أو أخري -غير معروفة بعد- أصبحت تعتمد علي الكائن الذي تتطفل عليه في الحصول علي الطاقة!
كما أن هناك كائنات تعيش بدون ضوء الشمس، كتلك التي تعيش حول فوهات البراكين في أعماق المحيطات (hydrothermal vents)، هذه الكائنات لا تعتمد علي التمثيل الضوئي (Photosynthesis) للحصول علي الطاقة ولكن تعتمد علي التمثيل الكيميائي (Chemosynthesis) أي إستخدام عناصر أخري من المعادن وغيرها للحصول علي الطاقة اللازمة لحياتها.
والحقيقة كلمة “شيء” في الآية الكريمة تتعدي معني الحياة، إذ لولا الماء لأصبح كوكب الأرض كوكبًا ميتاً بلا حراك لا يختلف كثيرًا عن أقرانه من الكواكب الصخرية في المجموعة الشمسية، فالقدرة علي نشأة واستمرار الحياة علي كوكب الأرض لبلايين السنين ترجع لسببين الأول هو إعادة التدوير، والثاني هو وجود آلية ضبط خصائص الحياة “Feedback Mechanisms” هذين الخاصيتين أعطيا للأرض صفة “الحياة” وهو ما أصبح يعرف بنظرية جايا “Gaia Hypothesis” التي كان أول من أقترحها الكيميائي جيمس لوفلوك “James Lovelock“، وهذه الصفة ما كانت لتحدث لولا وجود الماء.
الذي نريد أو نؤكد هو أنه لا يمكن لأي كائن حي العيش بدون ماء، فلا توجد خلية حية إلا وعماد وجودها هو الماء.
لكن هذا يستدعي عدد من التساؤلات:
-
متي ظهر الماء علي الأرض؟
-
وما مصدره؟
-
ولماذا الماء وليس أي سائل آخر كان هو السر وراء الحياة؟ بمعني آخر ما هي خصائص الماء التي جعلته سر الحياة علي الأرض
متى ظهرت المياه على الأرض؟
يتفق جميع علماء الأرض تقريبا على أن المياه كانت موجودة قبل أي شيء آخر، بل أن المياه لعبت دورًا حاسمًا في نشأة الكوكب نفسه، أي أنها كانت موجودة قبل وجود الكوكب!، وكما يقول فان ديشويك ” van Dishoeck”، أستاذ الفيزياء الفلكية الجزيئية في مرصد لايدن ” Leiden Observatory”، ورئيس الاتحاد الفلكي الدولي أن المياه ساعدت في ولادة الكواكب بطريقتين.[1]
“المياه في صورتها الغازية بمثابة المبرد الذي بسبب وجوده تتكثف الغازات البين نجمية لتصنع النجوم، بينما في صورتها الجليدية فهي تسهل التصاق جزيئات الغبار الصغيرة بعضها ببعض والتي في نهاية المطاف تصبح كويكبات ثم كواكب “[2]
وقد أمكن تجريبياً إثبات الدور الذي تلعبه المياه في نشأة النجوم،[3] ولذلك فإنه ليس من المستغرب أن المياه موجودة في كل مكان في جميع أنحاء الكون وفي العديد من الكواكب والأقمار،[4] حتى الفضاء بين النجوم يحتوي على المياه في أشكال مختلفة إما كغاز أو جليد، لكن علي الأرض فقط نشاهد المياه في أشكالها الثلاثة في درجة حرارة الكوكب الطبيعية.
ما هو مصدر الماء على الأرض؟
الجواب الصريح والموجز جدًا هو أننا لا نعرف، حتى وقت قريب كانت الإجابة الأكثر شيوعاً هي أن مصدر المياه علي الأرض جاء من خارجها بواسطة المذنبات أو الكويكبات (comets and asteroids) التي كانت بمثابة قرب ماء هائلة الضخامة، إلا أن هناك بعض الأدلة على أن رصيد الأرض من المياه كان قد تم أيداعه فيها منذ بداية نشأتها، ثم أفرجت عنه البراكين في صورة بخار الماء، لكن ربما الأرجح هو أن المياه علي الأرض لديها مصدرين، من داخل ومن خارج الأرض.
ومع ذلك ومهما كان المصدر فإن المهم في الأمر هو لماذا كانت هذه الكمية من المياه، التي تقدر بحوالي 332.5 مليون ميل مكعب،هي ما تحتاجه الأرض كي تصبح كوكباً صالحاً للسكن؟ وبغض النظر عن مدي دقة هذا الرقم، فإن السؤال هو لماذا لم يكن رصيد الأرض من المياه أكثر أو أقل مما هو عليه؟ من الذي اتخذ القرار بأن ما يكفي هو ما يكفي؟
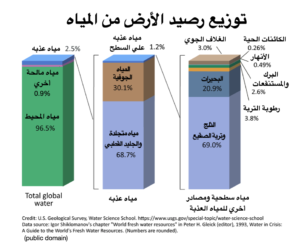
والحقيقة أنه ليست فقط كمية المياه وحدها هي التي تحتاج إلى قرار، بل أيضا نوعيتها وتوزيعها سواء علي سطح الأرض أو في باطنها (انظر الشكل 1).[5]
شكل رقم 1: يبين توزيع رصيد الأرض من المياه
خصائص الماء وملائمتها للحياة علي الأرض:
فما هي تلك الخصائص المعجزة للماء التي جعلت من الضرورة أن يكون هو-دوناً عن أي سائل آخر- أول مادة تتواجد علي سطح الأرض؟
هذه التساؤلات هي التي في عام 1832 كان عالم الطبيعة الإنجليزي ويليام ويويل ” William Whewell” يحاول العثور على إجابة لها، وبعد أن أكتشف أن بعض خصائص الماء تنتهك القواعد المعروفة للقانون الطبيعي، نشر كتابا تحت عنوان “علم الفلك والفيزياء العامة في اللاهوت الطبيعي “”“Astronomy and General Physics Considered with Reference to Natural Theology”. “، وكان الاستنتاج الذي خلص إليه هو أن التناقضات في الخصائص الحرارية للمياه ينبغي أن تؤخذ كدليل على أن هذه المادة قد أنشئت خصيصا من أجل الحياة.
الآن في القرن الحادي والعشرين، أصبحنا نعرف الكثير عن الماء، ليس فقط عن خواصه الحرارية ولكن أيضا عن خصائصه الكيميائية والفيزيائية بل أيضا عن تركيبه الجزيئي، الذي تبين أنه السر وراء ما عرف بالخصائص “الشاذة” للماء
https://youtu.be/UukRgqzk-KE
التركيب الجزيئي للمياه H2O:
المعروف أن جزيء الماء جزيء صغير يتكون من ذرة أكسجين وذرتين هيدروجين “H2O” متحدين معاً بما يعرف بالرابطة التساهمية (covalent bond) لأن الإلكترون في المدار الخارجي لكل من ذرتي الهيدروجين يتحول إلي إلكترون مشتركًا بينه وبين ذرة الأكسجين.
لكن الأمر لا يتوقف هنا، فجزيء الماء يوصف بأنه جزيء قطبي وذلك لأن له قطبين أحدهما سلبي هو جزيء الأكسجين والآخر إيجابي وهو جزيئي الهيدروجين، سبب هذا التباين في الشحنة هو أن ذرة الأكسجين، لو اعتبرنا أنها الأخ الأكبر لذرتي الهيدروجين، فإنها تستأثر بالإلكترونات المشتركة بينهما لفترة أطول والإلكترونات كما نعرف سالبة الشحنة وبالتالي تكتسب ذرة الأكسجين صفة السلبية بينما يحدث العكس بالنسبة للهيدروجين.
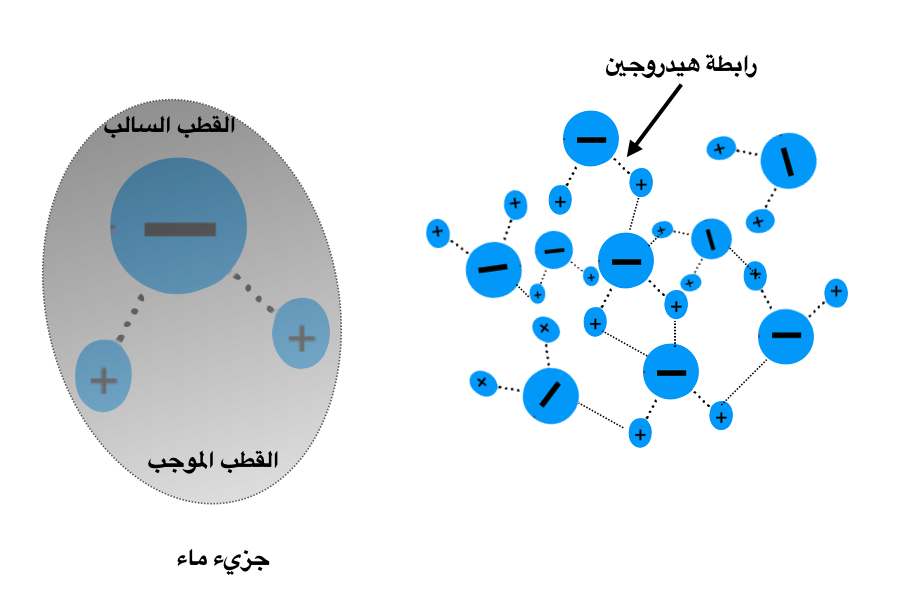
لذلك ترتبط جزيئات الماء ببعضها البعض، عن طريق رابطة الهيدروجين بحيث تكون النهايات السلبية مع النهايات الإيجابية والعكس بالعكس، وهذه الرابطة دائمًا في حالة تفكك وإعادة إرتباط تريليونات من المرات في الثانية الواحدة، وبالطبع نحن لا نري ذلك ولكن نري المياه في حالة سيولة وتتدفق بدون انقطاع (أنظر شكل 1).
هاتان الصفتان المميزتان وهما: الطبيعة القطبية لجزيئات الماء، ورابطة الهيدروجين القوية بين جزيئاته، وراء معظم الخصائص الكيميائية والفيزيائية والحرارية التي يتمتع بها الماء، والتي جعلته مادة فريدة من نوعها له من الخصائص التي يصفها العلماء بالشذوذ ليس فقط لتفرد المياه بها ولكن لشذوذها عن القواعد الفيزيائية المعروفة، وبعض العلماء عد ما لا يقل عن 60 خاصية من تلك الخصائص الشاذة، ولا يزال هناك العديد من خصائص الماء التي لم يتم اكتشافها بعد.
شكل رقم :1 الشكل علي اليمين يمثل التركيب القطبي لجزيء الماء، ذرة أكسجين وذرتين هيدروجين لكن بسبب أن ذرة الأكسجين، تستأثر بالإلكترونات السالبة الشحنة لفترة أطول إكتسب جزيء الماء صفة القطبية، والشكل علي اليسار يمثل كيفية إتحاد جزيئات الماء ببعضها البعض برابطة الهيدروجين، الرابطة بين الجزيئات تنفك وتعاد تنفك وتعاد تريليونات من المرات في الثانية الواحدة.
الخصائص الفيزيائية للمياه
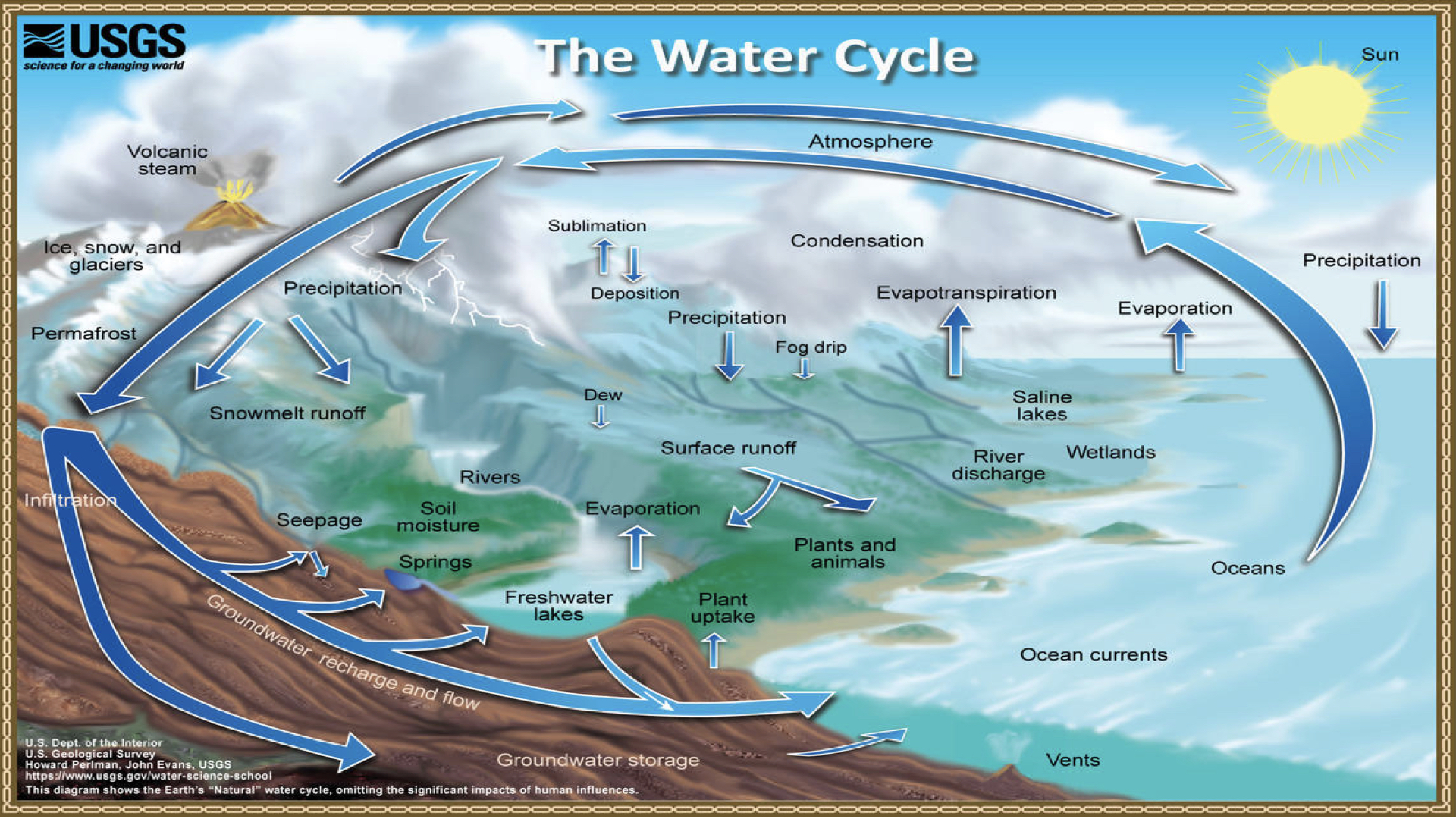
لعل أشهر خاصية فيزيائية للماء هي أنه المادة الوحيدة التي تتواجد بأشكالها الثلاثة الصلبة والسائلة والغازية في درجة حرارة الأرض الطبيعية بدون أي تغير في بنيتها الجزيئية، بسبب هذه الخاصية فان المياه لا تتوقف عن الدوران في جميع جنبات الأرض في كل وقت وفي كل مكان، لتبُث الحياة في كل ما علي الأرض، تمامًا مثل الدورة الدموية في جسد الكائن الحي والتي تصل لكل خلية من خلايا الجسم في جميع الأوقات (شكل 2).
شكل رقم 2: دورة الماء أو الدورة الهيدرولوجية الماء عنصرًا رئيسياً سواء في تشكيل الغلاف الجوي أو في ضبط المناخ أو لخلق تربة خصبة صالحة للزراعة وذلك من خلال دورانه المستمر بين جميع مكونات نظام الأرض فيما يعرف بدورة الماء أو بالدورة الهيدرولوجية (الشكل 2)، في هذه الدورة قد ينتقل جزيء الماء من حالة إلى أخرى في أقل من ثانية أو قد يستغرق الأمر ملايين السنين.[6] Credit to USGS-Public Domain
هناك أيضًا خاصيتين فيزيائيتين يتميز بهما الماء ولهما دورًا حيويًا في حياتنا هما التماسك والتلاصق :
الماء لدية قوة تماسك “Cohesion Force” مرتفعة: لأن جزيئات الماء جزيئات قطبية (Polar Molecules) فإنها ترتبط مع نفسها (ومع غيرها من الجزيئات القطبية)، بشبكة من الروابط الهيدروجينية التي تجعلها في حالة تجاذب مستمرة مع بعضها البعض من جميع الجوانب (راجع فصل 2)، لكن عند تلاقي سطح مائي مع وسط هوائي تتعرض الجزيئات السطحية لقوة جذب فقط من الجزيئات التي أسفل منها والمجاورة لها ولذلك يصبح سطح الماء وكأنه طبقة رقيقة من الجلد، وتعرف هذه الخاصية بالتوتر السطحي “Surface Tension” والماء يتمتع بأعلى درجات توتر سطحي بين جميع السوائل (باستثناء الزئبق)، وهذه الخاصية هي المسؤولة عن وجود الماء في شكل قطرات متماسكة، وربما بعضنا رأي أنواع من الحشرات تستطيع السير أو الوقوف أو حتي يحدث بينها تلاقي علي سطح الماء.
الخاصية الثانية الهامة هي خاصية التلاصق ” Adhesive Property” والتي بصفة عامة تعني جاذبية جزيء من مادة إلي جزيء من مادة أخري، وصحيح أن جزيئات الماء، كما ذكرنا، تنجذب لبعضها البعض ولكنها تنجذب أكثر إلي جزيئات مواد مختلفة خصوصًا إذا كان لها شحنة ما موجبة أو سالبة، وربما أغلبنا سمع عن تجربة الأنابيب الشعرية التي فيها إذا وضعنا أنبوبة دقيقة من الزجاج في حوض من الماء فسنري عمود الماء يرتفع وكأنه يتسلق داخل الأنبوبة وذلك بسبب انجذاب جزيئات الماء إلي جدار الأنبوب الزجاجي أكثر من انجذابها لبعضها البعض(التلاصق أقوي من التجاذب) (يرتفع الماء ضد الجاذبية -إلي حد معين- عندما تكون قوة التلاصق “Adhesion Force ” أقوي من قوة التجاذب بين الجزيئات “ Cohesion Force “).
بالطبع ظاهرة التوتر السطحي للماء كما ذكرنا تعتبر مهمة لبعض الكائنات، إلا أن أهميتها تكمن في كونها أيضًا حيوية لوظائف جيولوجية و بيولوجية أخري هامة.
فعلى سبيل المثال، كما رأينا في الفصل الثاني في كتابي( The Earth -Story of Design and Intentionality) فإن التجوية الفيزيائية وهي عملية هامة لتفتيت الصخور واستخراج العناصر المعدنية منها تعتمد على خاصية قوة تماسك جزيئات الماء، فقوة الجذب بين جزيئات الماء الذي يتسرب في شقوق الصخور الدقيقة هي التي تجعل منه وحدة واحدة وكأنه بالفعل وتد رُشق في الصخور، ثم عندما يتجمد ويتمدد تتضعضع الصخور وفي النهاية تتفتت مهما كانت صلابتها.
بينما من الناحية البيولوجية فإن خاصيتي تماسك جزيئات الماء والخاصية اللاصقة للماء يعتبرا معًا أمرًا حيويًا لحياة النباتات والأشجار، فبدون هاتين الخاصيتين لا يمكن أن يكون لدينا نباتات أطول من بضعة سنتيمترات، فهما الآلية التي بها يمكن أن يصل الماء إلي قمم أعلي الأشجار عبر أوعية النبات المائية الدقيقة، كما أن تبخر الماء من أوراق الأشجار يقوم بعمل جهاز جذب “أو شفط ” للمياه عبر تلك الأوعية، كلما زاد التبخر زاد معدل جذب المياه، وهكذا يصل الماء وما يحمله من غذاء إلي قمم الأشجار الطويلة بدون ضجيج أو مجهود عضلي أو مضخات أو روافع للمياه، ويقدر العلماء أنه في يوم مشمس يمكن للأشجار الطوال أن تنقل مئات الجالونات من التربة إلي الأوراق، بدون ضجيج ولا الحاجة لأي طاقة أو مجهود. [7]
وأخيرًا وليس آخرًا من أهم الخصائص الفيزيائية للماء هي أن درجة لزوجته “Viscosity” وتعرّف بأنها مقياس مقاومة السائل للتدفق والإنسياب وتعتمد علي درجة الإحتكاك بين جزيئات السائل، منضبطة بما يتناسب مع عديد من الوظائف في بيئات ليس لها أي علاقة ببعضها البعض:
-
فلا شك أن صعود المياه مئات الأمتار أوعية النبات المائية التي أشرنا إليها يعتمد علي درجة لزوجة منضبطة، وقبل ذلك فإن بقاء المياه في التربة هو الآخر يتطلب درجة لزوجة منضبطة، فلو كانت درجة لزوجة المياه أقل مما هي عليه فإن المياه ستتسرب من خلال مسام التربة بسرعة كبيرة جدًا ولن يكون هناك وقت كافي للنباتات للاستفادة منها ولا مما تحمله من المواد الغذائية والمعادن، ولو أنها كانت مرتفعة عن ما هي عليه (مثل الزيت) فلن ينتشر الماء في مسام التربة بالسهولة اللازمة، وأيضًا لن تصعد خلال أوعية النبات المائية الدقيقة كي تصل إلي جميع أطرافه.
-
أما علي مستوي الخلايا في الكائنات الحية فسنجد أن درجة اللزوجة التي كانت ضرورية لحمل الغذاء لأوراق الأشجار المرتفعة وتروية التربة، هي نفسها التي توفر الوسط المناسب داخل خلايا الكائنات الحية كي تستمر في وظيفتها، فلو زادت لزوجة الماء عن ما هي عليه لأعاقت التفاعلات الكيميائية داخل الخلايا، بينما لو كانت أقل لكانت حركات جزيئات العناصر في الخلايا حركة عشوائية مشابهة لما يعرف بالحركات البراونية ” Brownian movements” أي تلك الجزيئات التي تتحرك بدون أن تحقق التفاعل المطلوب. [8]
-
ولا ننسي أيضًا أن 90٪ من مكونات الدماء التي تجري في عروقنا هي من الماء، فأي تغيير في لزوجة الدم سواء عن طريق الزيادة أو النقصان من شأنه أن يؤثر بشكل خطير علي قدرة القلب علي الاستمرار في ضخ الدماء وبالتالي علي فعالية الدورة الدموية ووصول الدم إلي أنحاء الجسم المختلفة، ويعلق مايكل دانتون علي ذلك بقوله “لزوجة الماء هي عنصر آخر من كفاءة الماء لحياة الخلايا: ليست منخفضة جدا، ليست عالية جدا – فقط بالدرجة المطلوبة!” [9]
الخصائص الحرارية للمياه:
في الفصل الثاني من كتابي( The Earth -Story of Design and Intentionality) ناقشت أهمية خاصية الإحتواء الحراري للماء، وخاصية الحرارة الكامنة سواء في حالة غليان أو تجمد الماء، وعرفنا أهمية تلك الخصائص في الحفاظ على مناخ الأرض وجعلها صالحة للسكن، المدهش أن نفس هذه الخصائص هي التي تعتمد عليها حياتنا وحياة العديد من الكائنات.
المياه و” خاصية الاحتواء الحراري ” “ Heat Specific Capacity“10]
الاحتواء الحراري لأي مادة يعني قدرتها علي امتصاص الطاقة الحرارية، وبالطبع تختلف هذه القدرة من مادة لأخري، وإتفق العلماء علي اعتبار أن كمية الحرارة اللازمة لرفع درجة حرارة جرام واحد من مادة ما درجة واحدة مئوية مقياساً لدرجة الاحتواء الحراري للمادة، وتبين أن الماء يتمتع بأعلى درجة احتواء حراري بين جميع السوائل، والسبب في ذلك هو رابطة الهيدروجين بين جزيئات الماء، فإن امتصاص الماء للحرارة يعني أولًا تفكك رابطة الهيدروجين كي تتحرر جزيئات الماء ومن ثَم تزداد حركتها وترتفع درجة حرارة الماء، وعندما تنخفض الحرارة يعاد بناء رابطة الهيدروجين مرة أخري مما يؤدي إلي إنطلاق الطاقة.
النتيجة التطبيقية هي أن المحيطات علي الأرض تقوم بوظيفة الالواح الضخمة لتخزين الحرارة، فهي تمتص طاقة الشمس في النهار فترتفع درجة حرارة الماء ببطء وبدرجة أقل من ارتفاعها علي اليابسة (لا تنسي أيضًا أن المياه بعكس رمال اليابسة في حركة مستمرة)، ثم تبثها مرة أخري في الليل فتنخفض الحرارة أيضًا ببطء، بالطبع هذه الخاصية توفر بيئة مثالية للكائنات البحرية لأنها تحافظ علي معدل التباين بين أعلي وأقل درجة حرارة في الحدود المعقولة، أيضًا توفر بيئة جيدة لسكان المناطق الساحلية المتاخمة للمحيطات حيث يكون التباين بين درجة حرارة الجو أثناء النهار والليل أقل منه بكثير عن المناطق البعيدة عن الساحل.
ولأن الاحتواء الحراري للماء يقدر بخمسة أضعاف الاحتواء الحراري للرمال لذلك قد يصل الفارق في درجة حرارة اليابسة بين الأماكن الأكثر سخونة والأبرد إلى 140 درجة مئوية، بينما في البحر يتراوح هذا الفارق على الأكثر بين 15-20 درجة مئوية، ويرجع هذا الاختلاف جزئيا إلى ” خاصية الاحتواء الحراري “، وجزئيا إلى خاصية الحرارة الكامنة مع تبخر المياه والتي سنتحدث عنها لاحقًا في هذا الفصل.
يمكن مراجعة الفيديو https://youtu.be/Y3ATc9he254
الذي يهمنا هنا هو أنه لو أن مساحة اليابسة كانت أكبر مما هي عليه أو مساحة المحيطات أقل مما هي عليه لأصبحت الحياة علي الأرض، خصوصًا في المنطقة المدارية، أكثر صعوبة أو ستصبح محصورة في حدود المناطق الساحلية.[11]
الحرارة المقاسة و الحرارة الكامنة
من أجل فهم الكيفية التي تعمل بها التيارات الهوائية علي ضبط المناخ، علينا أولاً أن نتعرف علي اصطلاحين ونعرف ما المقصود بهما وهما الحرارة المقاسة و الحرارة الكامنة وهما من الخواص الحرارية للماء.[12]
المعروف أن ارتفاع درجة الحرارة لأي جسم تحدث نتيجة تسارع حركة جزيئاته، على سبيل المثال إذا أردنا أن نحول كمية من الماء إلي بخار فعلينا أن نضيف طاقة حرارية للماء فتتفكك جزيئات الماء من بعضها البعض وتتسارع حركتها ثم تبدأ في التبخر عندما تصل درجة الحرارة إلي مائة درجة مئوية “1000C ” وهي درجة غليان الماء وتلك هي الحرارة المقاسة أي الحرارة القابلة للقياس، ولكن حتي عندما نصل لتلك الدرجة فلن يتبخر الماء كله فجأة، بل علينا الاستمرار في إضافة مزيد من الطاقة من أجل أن يتحول كل الماء إلي بخار، لكن بالرغم من أضافتنا لمزيد من الطاقة إلا أن درجة حرارة المياه المقاسة لا ترتفع فوق مائة درجة، فأين ذهب ما أضفناه من طاقة؟ هي بالطبع لم تُفقد، الذي حدث أنها تستخدم في تفكيك روابط الهيدروجين بين جزيئات الماء حتى تتباعد عن بعضها ويتحول الماء كله إلى بخار، معني هذا أنه من أجل أن تتبخر المياه تمامًا اضطررنا أن نضيف طاقة حرارية فوق المائة درجة لكننا لا نستطع قياسها بالطرق العادية، وتلك هي الحرارة الكامنة، وقد تبين أن الماء يحتاج إلي حوالي 540 سعرة حرارية من الطاقة الكامنة، أي فوق طاقة الغليان، من أجل أن يتبخر وهذه لا شك كمية كبيرة من الحرارة الغير قابلة للقياس.
بالمثل إذا أردنا أن نحول جرامًا واحدًا من الماء إلى جليد، علينا أن نخفض درجة الحرارة إلى الصفر “00C ” التي هي درجة تجمد الماء العذب، ولكن مرة أخرى لن تتحول كل المياه إلى جليد في وقت واحد، ولكن علينا أن نستمر في عملية التبريد لبعض الوقت، وقد وجِد أنه خلال هذا الوقت لابد من إزاحة 800 (ثمانون) من السعرات الحرارية الإضافية فيما دون درجة التجمد وذلك حتي يتجمد الماء كله، هذه الحرارة الكامنة التي تم إزاحتها كانت ضرورية لإعادة ترتيب جزيئات الماء وحتي يتحول الماء من الحالة السائلة إلى الحالة الصلبة، هذه الحرارة الكامنة التي تم إزاحتها تنتشر لتدفئ الوسط المحيط بالماء.[13] (أنظر شكل رقم 2).
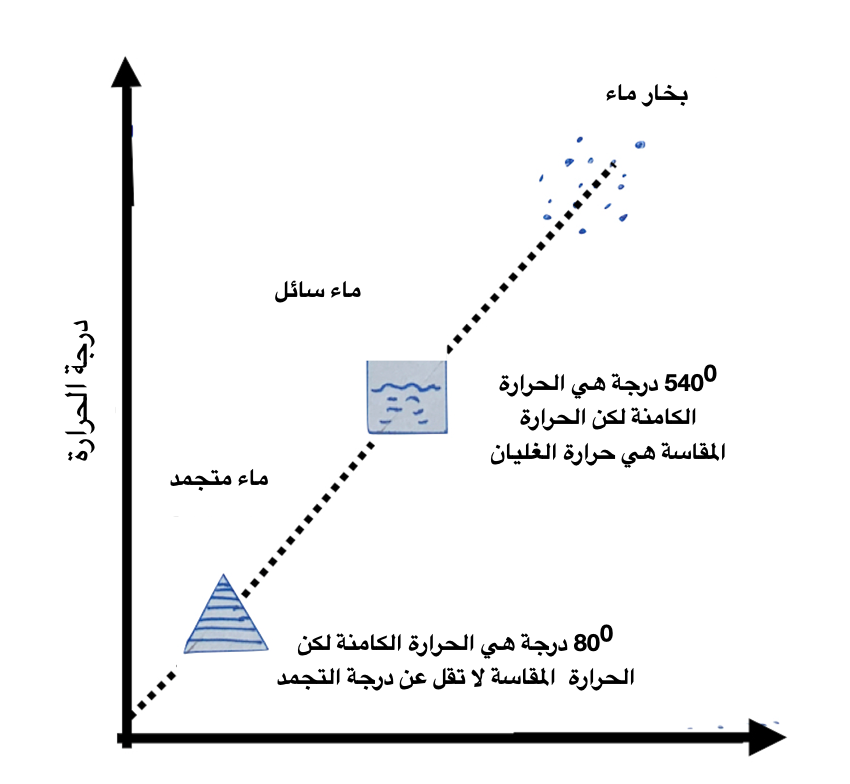
شكل رقم :2 الرسم يوضح العلاقة بين الحرارة الكامنة والحرارة المقاسة ، عند تحول الماء من صورة صلبة إلي سائل ثم إلي بخار.